bueno stoi probando a ver si se meter las cosas.feliz navidad
tripanosoma-y-leishmania-vet1103
Este es el blog que va a tratar sobre el tripanosoma y la leishmania. Ambos están en el reino de los protistas. Aceptamos sugerencias que tendrán que estar apoyadas por documentos. Posteriormente se votará en un lugar superscreto si se aceptan como verdaderos o no... Ahora en serio, si alguien sabe algo que nos lo diga, nos será de ayuda. Gracias. Pablo J. Andrés, Carlos Pueyo y Toni Corral
Thursday, December 28, 2006
Sunday, December 24, 2006
Leishmania
Taxonomía:
Reino Protista
Subreino Prtotozoa
Pyllum Sarcomastigophora
Subphyllum Mastigophora
Clase Zoomastigophorea
Suborden Kinetoplastida
Familia Trypanosomatidae
Género Leishmania
Morfología:
La forma intracelular, llamada amastigote afecta células del sistema retículo endotelial en el hospedero vertebrado.

El amastigote es ovalado o redondeado, inmóvil, mide de dos a cinco micrómetros, tiene un núcleo central y cerca está el cinetoplasto, en forma de barra y está asociado a un rudimento de flagelo que no se extiende fuera del parásito, el cual se conoce como rizoplasto.
El estadío presente en el hospedero invertebrado se denomina promastigote, es extracelular, alargado, aproximadamente veinte micrómetros de longitud, un núcleo central y un cinetoplasto terminal o subterminal en la parte anterior, del cual se origina un flagelo casi de igual tamaño que el cuerpo.
Ciclo de vida:
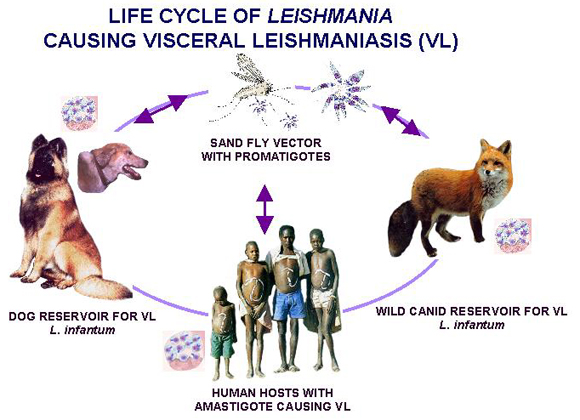
Los flebótomos al picar al hospedero vertebrado ingieren sangre y linfa que contiene amastigotes, estos sufren un cambio progresivo en el tracto digestivo del vector, hasta convertirse en formas alargadas que desarrollan un flagelo y se multiplican por fisión binaria (proceso que ocurre en zona diferente al tracto digestivo). La multiplicación se mantiene (promastigote) fuera desde ocho a veinte días según la especie. Una vez infectante, los promastigotes migran a la parte anterior del vector, desde donde son inoculados nuevamente en el momento en que se necesita una segunda alimentación.
En el interior del huésped vertebrado, los promastigotes son fagocitados por las células mononucleares y pierden su flagelo, transformándose en amastigotes, los cuales quedan incluidos dentro de una vacuola parasitofora que al unirse al lisosoma forma el fagolisosoma (teóricamente para la destrucción del microorganismo). Aquí comienza a multiplicarse hasta provocar lisis celular y excreción del microorganismo a células vecinas donde se repite el proceso.
Los flebótomos al picar al hospedero vertebrado ingieren sangre y linfa que contiene amastigotes, estos sufren un cambio progresivo en el tracto digestivo del vector, hasta convertirse en formas alargadas que desarrollan un flagelo y se multiplican por fisión binaria (proceso que ocurre en zona diferente al tracto digestivo). La multiplicación se mantiene (promastigote) fuera desde ocho a veinte días según la especie. Una vez infectante, los promastigotes migran a la parte anterior del vector, desde donde son inoculados nuevamente en el momento en que se necesita una segunda alimentación.
En el interior del huésped vertebrado, los promastigotes son fagocitados por las células mononucleares y pierden su flagelo, transformándose en amastigotes, los cuales quedan incluidos dentro de una vacuola parasitofora que al unirse al lisosoma forma el fagolisosoma (teóricamente para la destrucción del microorganismo). Aquí comienza a multiplicarse hasta provocar lisis celular y excreción del microorganismo a células vecinas donde se repite el proceso.

Leishmaniosis:
Este es el nombre de la enfermedad que causa el microorganismo problema. La Leishmaniosis existe en tres formas principales: cutánea (más abundante), muco cutánea y visceral.
De forma general produce ulceras en la piel que pueden tardar en sanar. Puede comprometer la mucosa de la oronasofaringe y causa lesiones deformantes. La forma más severa (visceral) provoca lesiones en bazo, hígado, medula ósea y ganglios linfáticos y es generalmente mortal.
En las formas zoonóticas las lesiones por lo general curan de manera espontánea y el hospedero queda posteriormente protegido, pero en el caso de los humanos se necesita tratamiento posterior porque constituyen reservorio de la infección.
La Leishmaniosis cutánea tiene diferentes formas de presentación según la zona geográfica en que se presente:
Este es el nombre de la enfermedad que causa el microorganismo problema. La Leishmaniosis existe en tres formas principales: cutánea (más abundante), muco cutánea y visceral.
De forma general produce ulceras en la piel que pueden tardar en sanar. Puede comprometer la mucosa de la oronasofaringe y causa lesiones deformantes. La forma más severa (visceral) provoca lesiones en bazo, hígado, medula ósea y ganglios linfáticos y es generalmente mortal.
En las formas zoonóticas las lesiones por lo general curan de manera espontánea y el hospedero queda posteriormente protegido, pero en el caso de los humanos se necesita tratamiento posterior porque constituyen reservorio de la infección.
La Leishmaniosis cutánea tiene diferentes formas de presentación según la zona geográfica en que se presente:
Diagnóstico
La presencia de una o mas úlceras cutáneas con las características apropiadas en una región endémica es sugestiva de leishmaniasis. El diagnóstico final dependerá de la identificación de amastigotes en frotis teñidos de raspados de la base de la úlcera o de especimenes de biopsia.
Leishmaniasis cutánea del Viejo Mundo
Hay formas cutáneas muy dramáticas; los pacientes presentan deformaciones consistentes en grandes nodulaciones, mismas zonas donde se encuentran a los parásitos; este tipo de leishmaniasis se divide en: L. tropica, L. major y L. aethiopica. El período de incubación de la leishmania cutánea varía de dos semanas a varios meses y en algunos casos hasta años, no es posible determinar la especie infectiva con las características de las lesiones; éstas se pueden iniciar como una pápula en el sitio en el que los promastigotes son inoculados. Gradualmente la pápula aumenta de tamaño, forma costra y por último se ulcera; por lo general ésta es superficial, circular con bordes eritematosos alcanzando un diámetro de 2 cm a más con salida de secreción serosa o seropurulenta.
-Tratamiento
Dependerá de la localización y la extensión de la lesión; cuando son grandes se utilizan preparados de antimonio pentavalente. Se ha empleado la pentamilina y la anfotericina B cuando los casos fracasan a la terapia con antimonio. Se ha recurrido a la aplicación tópica de paramomicina para el tratamiento de infecciones cutáneas y se ha mencionado la utilidad del ketoconazol a dosis de 200 - 400 mg/día durante seis semanas.
Leishmaniasis cutánea del Nuevo Mundo
También denominada leishmaniasis americana, está difundida en Latinoamérica y los agentes etiológicos son: L. braziliensis, L. panamensis y L. mexicana. El espectro de la enfermedad comprende úlceras cutáneas aisladas, localizadas. La leishmaniasis cutánea difusa debida a L. braziliensis es la única forma de leishmaniasis cutánea americana con elevada mortalidad. En este trastorno el compromiso de la nariz, la cavidad oral y la faringe es a veces tan destructivo y mutilante que el individuo no puede comer. Sin embargo la variedad de manifestaciones dermatológicas varían de pequeñas lesiones costrosas, secas a grandes lesiones anteriormente descritas. De las leishmaniasis cutáneas, la más importante en nuestro medio es la úlcera de los chicleros; el artrópodo trasmisor es del género Phebotomus y las lesiones se caracterizan por la aparición de una pápula que evoluciona a nódulo y luego ulcera el pabellón auricular; la evolución es muy crónica.
-Tratamiento
Los fármacos de primera elección son los compuestos de antimonio pentavalente; la mayor experiencia en Latinoamérica ha sido con antimoniaco de meglumina. Se han empleado diversos esquemas terapéuticos: 20 mg/kg de peso durante 20 días. Los pacientes que no responden pueden ser tratados con anfotericina B o bien el isetianato
de pentamida; recientemente se ha utilizado el interferón gamma recombinante. Se han administrado otros fármacos como el itraconazol y el alopurinol; sin embargo la experiencia no es aún suficiente con estos medicamentos.
La Leishmaniosis mucocutánea se asemeja a la lepra por su forma de presentación, destruye tabique nasal y cavidad oral. Puede presentarse seguido o hasta veinte años después de la cutánea. El tratamiento es largo y a menudo requiere cirugía reconstructiva.
La Leishmaniosis visceral es endémica en la India (llamada kala azar). La mortalidad se estima entre cincuenta mil y doscientos mil personas al año. La evidencia en adultos es ligeramente superior que en niños. En éstos comienza por fiebre y esplenomegalia seguido por edema en miembros inferiores, palidez de piel y mucosa, anemia, leucopenia y trombocitopenia, puede haber estomatitis.
de pentamida; recientemente se ha utilizado el interferón gamma recombinante. Se han administrado otros fármacos como el itraconazol y el alopurinol; sin embargo la experiencia no es aún suficiente con estos medicamentos.
La Leishmaniosis mucocutánea se asemeja a la lepra por su forma de presentación, destruye tabique nasal y cavidad oral. Puede presentarse seguido o hasta veinte años después de la cutánea. El tratamiento es largo y a menudo requiere cirugía reconstructiva.
La Leishmaniosis visceral es endémica en la India (llamada kala azar). La mortalidad se estima entre cincuenta mil y doscientos mil personas al año. La evidencia en adultos es ligeramente superior que en niños. En éstos comienza por fiebre y esplenomegalia seguido por edema en miembros inferiores, palidez de piel y mucosa, anemia, leucopenia y trombocitopenia, puede haber estomatitis.
Los amastigotes se encuentran en los macrófagos de todo el sistema reticuloendotelial; el agente etiológico es L. donovani aunque en otras ocasiones se aíslan otras especies de Leishmania. Los síntomas y los hallazgos representan un espectro de la enfermedad ya que podemos encontrar manifestaciones francas como fiebre, esplenomegalia, hepatomegalia, leucopenia, hipergammaglobulinemia y pérdida de peso. Por otra parte la enfermedad se puede manifestar en forma asintomática que incluso se llega a resolver por sí misma o presentando una evolución latente. Habrá que señalar que la leishmaniasis es una infección oportunista en sujetos con supresión de la inmunidad celular
Labels: leishmania
Trypanosoma Rangeli
Además del trypanosoma cruzi existe también el trypanosoma rangeli,que a diferencia del cruzi
no es patógeno para los hospederos vertebrados pero sí para los invertebrados.
Les causa la muerte a largo plazo, por la obstrucción que le produce en las glándulas salivares y la dificultad para obtener la suficiente ingesta de sangre, que le impide llevar a cabo las mudas en sus diferentes estados del desarrollo.
Geografía
Trypanosoma rangeli presenta una distribución geográfica que se superpone con la de T. cruzi, compartiendo en muchos casos el mismo insecto vector y también reservorios comunes, lo que conlleva a la ocurrencia de infecciones mixtas tanto en los vectores como en los hospederos vertebrados.
Interés
T. rangeli representa interés médico como posible fuente de confusión en el diagnóstico de la enfermedad de Chagas por la reactividad cruzada con T. cruzi, debido a que ambos parásitos poseen antígenos comunes.
Ciclo de vida en el hospedero vertebrado:
 Aunque se han encontrado formas de T. rangeli en sangre de humanos y en varias especies animales silvestres y domésticas, el ciclo de vida en el hospedero vertebrado sigue sin ser aclarado y los informes en la literatura son escasos y controversiales. Se le ha encontrado circulando en sangre en su forma de tripomastigote, sin embargo no se ha podido encontrar células infectadas in vivo con este parásito, aunque en experimentos de infección celular in vitro sí ha sido posible observar las formas intracelulares del parásito. Algunos autores han evidenciado ausencia de multiplicación de T. rangeli in vitro en diferentes líneas celulares. Sin embargo, otros autores, han informado la presencia de parásitos intracelulares y su multiplicación en la línea celular VERO de una cepa colombiana de T. rangeli.
Aunque se han encontrado formas de T. rangeli en sangre de humanos y en varias especies animales silvestres y domésticas, el ciclo de vida en el hospedero vertebrado sigue sin ser aclarado y los informes en la literatura son escasos y controversiales. Se le ha encontrado circulando en sangre en su forma de tripomastigote, sin embargo no se ha podido encontrar células infectadas in vivo con este parásito, aunque en experimentos de infección celular in vitro sí ha sido posible observar las formas intracelulares del parásito. Algunos autores han evidenciado ausencia de multiplicación de T. rangeli in vitro en diferentes líneas celulares. Sin embargo, otros autores, han informado la presencia de parásitos intracelulares y su multiplicación en la línea celular VERO de una cepa colombiana de T. rangeli.Relación filogenética entre T. rangeli y T. cruzi:
En ausencia de evidencia paleontológica, la historia del orden kinetoplastidia ha sido reconstruida a partir de estudios comparativos de la morfología, los ciclos de vida y la distribución de los hospederos. Teniendo en cuenta evidencias y estudios recientes es posible demostrar el origen monofilético de Trypanosomatidae; de esta manera un flagelado ancestral de las plantas o de un insecto pasó a los mamíferos cuando éste fue ingerido por un marsupial omnívoro, migrando a sus glándulas anales. En este tipo de hipótesis tenemos un parásito primitivo asociado con un marsupial, los tripanosomátidos probablemente se transmitían directamente entre los reservorios actuales a través de las secreciones de las glándulas anales y la orina, tal como lo ha enunciado Deane.
Una posterior adaptación a la forma sanguínea, pudo surgir cuando el parásito fue capaz de transmitirse con ayuda de un insecto hematófago. Así, algunos insectos predadores del orden Reduviidae, desarrollaron la capacidad de tomar sangre de los mamíferos, lo cual permitió que Trypanosoma sp primitivo pudiera dispersarse a otros hospederos tales como ratones, armadillos y murciélagos.
Por otro lado, la posición taxonómica y las relaciones evolutivas de T. rangeli con T. cruzi son controversiales y aún no se han podido dilucidar completamente. Al nivel de morfología y comportamiento, T. rangeli es clasificado dentro del subgénero Herpetosoma, pero caracterizaciones bioquímicas usando diferentes marcadores han permitido concluir que la ruta de transmisión que en un principio fue utilizada para la clasifi cación, actualmente, no tiene ningún tipo de validez y es un carácter con poca importancia evolutiva.
Labels: Trypanosoma rangeli
Tripanosoma cruzi, el invasor
Morfología
El parásito de la enfermedad de Chagas es un protozoario microscópico -animal de una sola célula, de aspecto muy simple visto en el microscopio óptico común-. Su nombre científico es Trypanosoma cruzi y está emparentado con otro microorganismo que, en África, provoca la "enfermedad del sueño", transmitida por la mosca "Tse-tse".
El T. cruzi es muy pequeño (mide aproximadamente 20 milésimos de milímetro) y posee un cuerpo alargado y provisto de un flagelo y una membrana ondulante, estructuras que, agitándose y vibrando, permiten su movilización dentro de la masa de sangre.
Las poblaciones de T. cruzi circulan en la naturaleza entre el hombre, el vector y los reservorios. A lo largo de su ciclo evolutivo sufren profundas alteraciones de forma que, de modo general, reflejan su adaptación al medio en que se localizan. Esas formas reciben nombres diferentes en función de su aspecto general, de la manera como el flagelo emerge del cuerpo celular y de la posición relativa de dos importantes estructuras intracelulares: el núcleo y el cinetoplasto ("órgano de movimiento").
Bajo condiciones experimentales, distintos aislamientos de T. cruzi tienen un tropismo diferente hacia diversos tejidos, pero en realidad residen predominantemente en el sistema retículo-endotelial, musculatura cardíaca y esquelética. Muchos han sido los estudios sobre la composición química y el metabolismo del parásito. Se sabe que el contenido en proteínas de las formas epimastigotes es de alrededor del 50% y el de lípidos de hasta un 20%. El T. cruzi metaboliza la glucosa y otros azúcares, realizando una fermentación aeróbica con excreción de ácidos orgánicos.
La composición antigénica del T. cruzi es compleja pero, a diferencia de los tripanosomas africanos, no presenta mecanismos de variación. La obtención de anticuerpos monoclonales (provenientes de la información genética de una célula inmune), el clonado del ADN y la posterior producción de moléculas del parásito, han contribuido a la identificación, caracterización y purificación de antígenos de interés biológico y de aquellos usados como marcadores de distintas cepas del parásito.
Transmisión
El parásito transmitido al hospedador vertebrado en las heces de la vinchuca es llamado en esta etapa tripomastigote metacíclico. Los tripomastigotes pueden invadir inmediatamente las células en la puerta de entrada o pueden ser transportados en la sangre a otros sitios antes de invadir las células del hospedador. Dentro de estas células se transforman en formas amastigotes que se multiplican rápidamente. Los amastigotes son redondeados con un flagelo externo muy corto o inexistente. El desarrollo de amastigotes a tripomastigotes se iniciaría después de cumplirse un número preprogramado de divisiones intracelulares, al cabo de las cuales la célula hospedera se destruye y los tripomastigotes entran en el torrente sanguíneo (tripomastigotes sanguíneos). Los tripomastigotes encontrados en la sangre circulante, de un tamaño total que varía entre 15 y 20m tienen flagelo libre, un cinetoplasto voluminoso, terminal o subterminal que contiene el 30% del ADN del parásito, y un núcleo oval. Estos tripomastigotes pueden infectar otras células, pero no son capaces de multiplicarse en la sangre ya que la única forma replicativa en el vertebrado es la forma amastigote intracelular.
Las vinchucas nacen del huevo libres de infección, se infectan al alimentarse del hombre o de los animales domésticos o silvestres infectados. Los tripomastigotes migran al intestino medio del insecto donde se transforman en epimastigotes, flagelados anchos, muy móviles, con el cinetoplasto entre el núcleo y el flagelo libre. Allí se dividen un gran número de veces. Las vinchucas quedan infectadas de por vida. Los epimastigotes se transforman en tripomastigotes metacíclicos y migran al intestino posterior de donde son excretados con las heces en el momento de la picadura. Mediante la degradación del ADN del cinetoplasto con enzimas restrictivas y su posterior análisis electroforético es posible la identificación de diferentes cepas de T. cruzi.
Enfermedad
La infección por T. cruzi modifica en forma generalizada el sistema inmune. Se ha descripto una severa inmunodepresión en pacientes en fase aguda aunque en ésta se producen anticuerpos. Los anticuerpos pueden contribuir a la fagocitosis y participan en la destrucción de los parásitos. El número de parásitos en sangre se ve así disminuido, pero el hospedador, de no mediar tratamiento adecuado, quedará infectado de por vida.. Los macrófagos pueden destruir al T. cruzi, pero son parasitados por este organismo. Se ha demostrado en estudios experimentales que la respuesta inmune celular es necesaria para el desarrollo de inmunidad contra el parásito. En la fase crónica de la enfermedad existe un restablecimiento de la respuesta inmune, que en muchos casos sería suficiente para poder controlar las manifestaciones de la enfermedad.
Vacuna
La posibilidad de obtener protección contra T. cruzi ha constituido uno de los principales anhelos de muchos investigadores. Se han usado como inmunógenos, parásitos vivos atenuados, muertos, fracciones subcelulares, macromoléculas y otros flagelados análogos. Las características de la enfermedad han mostrado, sin embargo, que la obtención de antígenos protectores es difícil. Existen mecanismos de agresión por antígenos de T. cruzi a los tejidos del hospedador, en los que probablemente exista una participación del sistema inmune, y hay evidencias de reacción cruzada entre T. cruzi y tejidos cardíacos y nerviosos. La existencia de estos mecanismos señala la necesidad de investigar antígenos de fracciones subcelulares o antígenos definidos que protejan ante un desafío parasitario, sin efectos agresivos, lo que se está desarrollando en varios laboratorios en la búsqueda de una vacuna.
La sensibilidad del T. cruzi a los quimiofármacos es tan baja que se halla muy cerca del efecto tóxico para el humano.
Morfología
El parásito de la enfermedad de Chagas es un protozoario microscópico -animal de una sola célula, de aspecto muy simple visto en el microscopio óptico común-. Su nombre científico es Trypanosoma cruzi y está emparentado con otro microorganismo que, en África, provoca la "enfermedad del sueño", transmitida por la mosca "Tse-tse".
El T. cruzi es muy pequeño (mide aproximadamente 20 milésimos de milímetro) y posee un cuerpo alargado y provisto de un flagelo y una membrana ondulante, estructuras que, agitándose y vibrando, permiten su movilización dentro de la masa de sangre.
Las poblaciones de T. cruzi circulan en la naturaleza entre el hombre, el vector y los reservorios. A lo largo de su ciclo evolutivo sufren profundas alteraciones de forma que, de modo general, reflejan su adaptación al medio en que se localizan. Esas formas reciben nombres diferentes en función de su aspecto general, de la manera como el flagelo emerge del cuerpo celular y de la posición relativa de dos importantes estructuras intracelulares: el núcleo y el cinetoplasto ("órgano de movimiento").
Bajo condiciones experimentales, distintos aislamientos de T. cruzi tienen un tropismo diferente hacia diversos tejidos, pero en realidad residen predominantemente en el sistema retículo-endotelial, musculatura cardíaca y esquelética. Muchos han sido los estudios sobre la composición química y el metabolismo del parásito. Se sabe que el contenido en proteínas de las formas epimastigotes es de alrededor del 50% y el de lípidos de hasta un 20%. El T. cruzi metaboliza la glucosa y otros azúcares, realizando una fermentación aeróbica con excreción de ácidos orgánicos.
La composición antigénica del T. cruzi es compleja pero, a diferencia de los tripanosomas africanos, no presenta mecanismos de variación. La obtención de anticuerpos monoclonales (provenientes de la información genética de una célula inmune), el clonado del ADN y la posterior producción de moléculas del parásito, han contribuido a la identificación, caracterización y purificación de antígenos de interés biológico y de aquellos usados como marcadores de distintas cepas del parásito.
Transmisión
El parásito transmitido al hospedador vertebrado en las heces de la vinchuca es llamado en esta etapa tripomastigote metacíclico. Los tripomastigotes pueden invadir inmediatamente las células en la puerta de entrada o pueden ser transportados en la sangre a otros sitios antes de invadir las células del hospedador. Dentro de estas células se transforman en formas amastigotes que se multiplican rápidamente. Los amastigotes son redondeados con un flagelo externo muy corto o inexistente. El desarrollo de amastigotes a tripomastigotes se iniciaría después de cumplirse un número preprogramado de divisiones intracelulares, al cabo de las cuales la célula hospedera se destruye y los tripomastigotes entran en el torrente sanguíneo (tripomastigotes sanguíneos). Los tripomastigotes encontrados en la sangre circulante, de un tamaño total que varía entre 15 y 20m tienen flagelo libre, un cinetoplasto voluminoso, terminal o subterminal que contiene el 30% del ADN del parásito, y un núcleo oval. Estos tripomastigotes pueden infectar otras células, pero no son capaces de multiplicarse en la sangre ya que la única forma replicativa en el vertebrado es la forma amastigote intracelular.
Las vinchucas nacen del huevo libres de infección, se infectan al alimentarse del hombre o de los animales domésticos o silvestres infectados. Los tripomastigotes migran al intestino medio del insecto donde se transforman en epimastigotes, flagelados anchos, muy móviles, con el cinetoplasto entre el núcleo y el flagelo libre. Allí se dividen un gran número de veces. Las vinchucas quedan infectadas de por vida. Los epimastigotes se transforman en tripomastigotes metacíclicos y migran al intestino posterior de donde son excretados con las heces en el momento de la picadura. Mediante la degradación del ADN del cinetoplasto con enzimas restrictivas y su posterior análisis electroforético es posible la identificación de diferentes cepas de T. cruzi.
Enfermedad
La infección por T. cruzi modifica en forma generalizada el sistema inmune. Se ha descripto una severa inmunodepresión en pacientes en fase aguda aunque en ésta se producen anticuerpos. Los anticuerpos pueden contribuir a la fagocitosis y participan en la destrucción de los parásitos. El número de parásitos en sangre se ve así disminuido, pero el hospedador, de no mediar tratamiento adecuado, quedará infectado de por vida.. Los macrófagos pueden destruir al T. cruzi, pero son parasitados por este organismo. Se ha demostrado en estudios experimentales que la respuesta inmune celular es necesaria para el desarrollo de inmunidad contra el parásito. En la fase crónica de la enfermedad existe un restablecimiento de la respuesta inmune, que en muchos casos sería suficiente para poder controlar las manifestaciones de la enfermedad.
Vacuna
La posibilidad de obtener protección contra T. cruzi ha constituido uno de los principales anhelos de muchos investigadores. Se han usado como inmunógenos, parásitos vivos atenuados, muertos, fracciones subcelulares, macromoléculas y otros flagelados análogos. Las características de la enfermedad han mostrado, sin embargo, que la obtención de antígenos protectores es difícil. Existen mecanismos de agresión por antígenos de T. cruzi a los tejidos del hospedador, en los que probablemente exista una participación del sistema inmune, y hay evidencias de reacción cruzada entre T. cruzi y tejidos cardíacos y nerviosos. La existencia de estos mecanismos señala la necesidad de investigar antígenos de fracciones subcelulares o antígenos definidos que protejan ante un desafío parasitario, sin efectos agresivos, lo que se está desarrollando en varios laboratorios en la búsqueda de una vacuna.
La sensibilidad del T. cruzi a los quimiofármacos es tan baja que se halla muy cerca del efecto tóxico para el humano.
Tripanosomiasis animal
Otras especies y sub-especies del género Trypanosoma, son patogénicas a los animales y causan tripanosomiasis animales en muchas especies animales salvajes y domésticas. En el ganado la enfermedad es conocida como Nagana(que significa “estar deprimido/alicaído”).
Los animales pueden ser hospedadores del patógeno humano, especialmente T.b. rhodesiense; es por ello que los animales domésticos y salvajes son importantes reservorios de parásitos. Los animales pueden ser infectados también por T.b. gambiense, sin embargo el rol epidemiológico preciso de estos reservorios no es bien claro. Esta enfermedad mata a los animales.
La enfermedad en animales domésticos y particularmente en ganado es un obstáculo importante en el desarrollo económico de las áreas rurales afectadas.
Clasificación
La clasificación del tripanosoma cruzi es la siguiente:
Reino Protista
Clasificación
La clasificación del tripanosoma cruzi es la siguiente:
Reino Protista
Filo Euglenozoa
Clase Kinetoplastidia
Orden Trypanosomatidae
Género Tripanosoma
Especie T.Cruzi
Labels: Tripanosoma cruzi



